日本:全球首款光免疫疗法药物获批,癌症新疗法—光免疫疗法有望加速
关于光免疫疗法,日本就医网从2018年开始一直在跟踪报道。作为术手,放疗、化疗和免疫治疗之后的“第种五治疗方法”,光免疫疗法自提出以来一直备受关注。
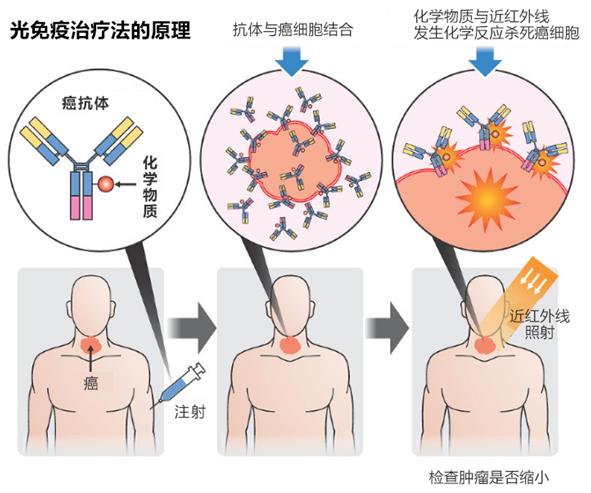
该疗法由美国国立卫生研究院(NIH)主任研究员小林久隆团队开发,其基本原理是:给患者注射可与近红外线反应的特殊光免疫药物,该药物会与癌细胞特有的蛋白质(抗体)结合,然后经体外或通过内窥镜利用近红外线照射肿瘤病灶,光线会破坏已经与化学物质结合的癌细胞的细胞膜,从而灭杀癌细胞。
此前,光免疫疗法已经进入临床试验,主要用于头颈部肿瘤的治疗。近日再传佳报,全球首款光免疫疗法药物—Akalux®(学名:Cetuximab Saratolacan Sdoium,简称Akalux®)在日本获批,用于治疗头颈部恶性肿瘤。该药物由日本乐天医药研发,已经于2020年9月下旬获得日本厚生劳动省的生产及销售许可,可用于「无法切除的局部晚期或局部复发性头颈癌」。与此药物搭配使用的「BioBlade® Laser System」(简称“BioBlade®”)的生产及销售许可也于2020年9月2日获批。早在去年4月,日本厚生劳动省将Akalux®列为先行审查指定项目(SAKIGAKE) ;而今年3月,乐天医药正式提出申请。如今,日本将成为首个获得核准制造和销售Akalux®的国家。
日本于2017年引入光免疫治疗临床试验,小林久隆团队与日本乐天医药正在共同研发一种名为Illuminox™的治疗技术平台,基于光免疫治疗的治疗原理,可以选择性地将光敏剂(即光免疫药物)携带到特定细胞,再透过照射光线来选择性地杀死癌细胞。以Illuminox™平台为基础所开发的第一种治疗方法为Akalux®和BioBlade®。
据悉,本次获批是基于针对局部复发性头颈癌的国外I / IIa期临床试验(39例)和日本I期临床试验(3例)的结果。在IIa期临床试验中,最佳缓解率为43.3%,其中4例(13.3%)完全缓解,9例(30.0%)部分缓解。在日本I期临床研究中,经中央独立审查判断的缓解率为66.7%(2位),均为部分缓解。
在日本,一般而言,医药品获得认可后将在60-90天内确定药物价格,并被收录进医疗保险范围之中。也就是说,预计最快今年内,可以在日本的医院内使用Akalux治疗。日本就医网也会一如既往的关注光免疫疗法,及时分享最新动态。


