日本的抗肿瘤病毒疗法开发
2019年诺华制药的CD19嵌合抗体CAR-T疗法在日本上市,除了其治疗滤泡性淋巴瘤的完全缓解率达到65%,总缓解率达到83%的高有效率受到关注,高达3,350万日元的治疗费用也令人结舌。2021年6月日本政府承认了东京大学开发的GΔ47溶瘤病毒治疗脑肿瘤,但严格限制了使用条件和药物许可时间。这是世界上第一个正式上市的抗肿瘤病毒疗法。
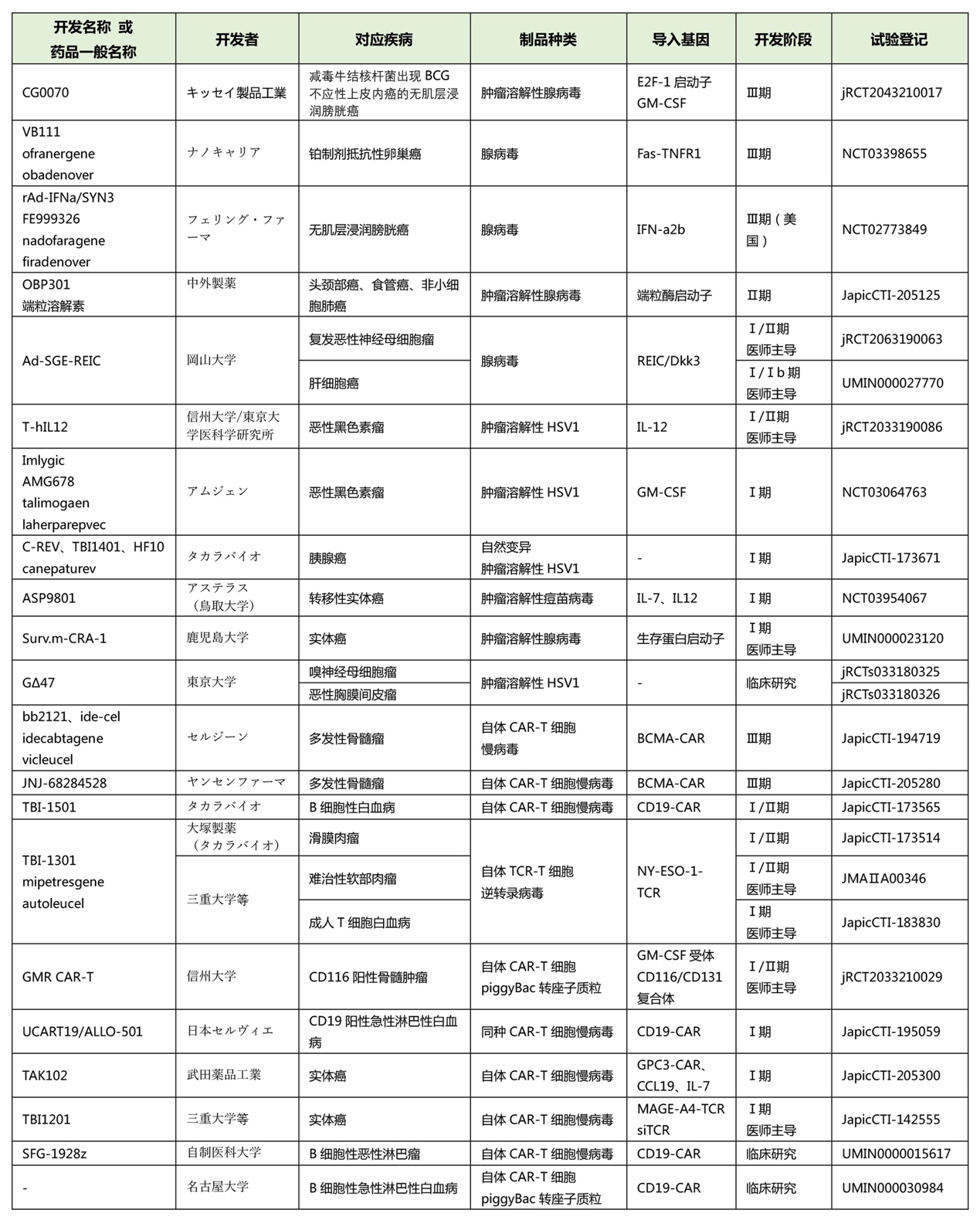
病毒疗法也属于免疫疗法,理论上容留病毒是治疗实体癌症最有效的方法,现在该领域的药品开发竞争越发激烈。用病毒感染肿瘤,使之溶解消褪。世界各国使用病毒溶解实体肿瘤已经研究了很多年(100年前就开始尝试了),人们发现使用已有病毒治疗恶性肿瘤疗效非常有限,而进行过基因改造的病毒却十分值得期待。日本政府批准的溶瘤病毒Δ47除了治疗脑肿瘤,也可治疗其他实体肿瘤,目前正在进行临床试验。日本就医网盘点了一下日本正在开发的病毒产品,截止到2021年8月的信息如下表。
1. 肿瘤溶解病毒GΔ47
肿瘤溶解性病毒GΔ47是以疱疹病毒1型(HSV1)为骨架的重新编辑基因的病毒。因为它只在胶质母细胞瘤细胞中增殖并发挥细胞毒活性,对正常细胞几乎没有影响。它是由东京大学医学科学研究所教授藤堂具紀开发并由第一三共制成药品投入实际应用。
日本国内的II期研究的中期分析显示GΔ47的胶质母细胞瘤患者1年生存率为92.3%,效果良好。根据日本药品和医疗器械管理局(PMDA)2021年5月13日的审查报告,从提交的材料来看该产品对恶性胶质瘤具有一定疗效,安全性尚可。但由于目前信息有限,即使在批准生产和使用后仍需继续评估和确认该产品的有效性和安全性。安全性方面,本品单独或与替莫唑氨联合治疗复发胶质母细胞瘤时,需要注意的不良反应有免疫反应相关的症状、骨髓抑制、发作痉挛、脑水肿和颅内肿瘤出血。基于上述资料,日本政府同意将本品纳入社保目录,8月12日定价1,431,918日元,1ml/1瓶。本品的有效性未经Ⅲ期临床试验验证,属于期待许可药品(验证无效将下架),2021年11月1日开始在指定医疗机构开始投入使用,需要继续记录2年的治疗成绩。因为胶质母细胞瘤治疗手段有限,人们对本品给予了很大的期待。
2.端粒溶解蛋白(OBP-301)
OBP-301是日本冈山大学消化器官外科教授藤原俊義开发的肿瘤溶解病毒制品。2019年经协议由中外制药独家开发和生产。OBP-301是一种包含端粒酶基因的限制增殖性腺病毒,应肿瘤细胞的端粒酶活性高,本品和区别正常细胞,选择性在肿瘤中增殖并破坏肿瘤。但本品对骨髓正常细胞(端粒酶活性高)有影响,临床试验中显示了一定的骨髓功能下降。在高龄,只可接受放疗的食管癌患者参加的临床试验中测算除了可使用OBP-301的剂量,2019年4月日本批准使用,2020年6月美国FDA品准用于罕见病。副反应可控,但疗效方面还需等待临床试验的结果。正在开发的新一代制剂为针对p53变异的腺病毒,药品开发代号为OBP-702。临床前试验已经确认端粒溶解蛋白有很强的抗肿瘤活性,破坏间质细胞的能力也很强。正准备启动骨肉瘤、直肠癌、胰腺癌的临床试验。
3.仙台病毒
仙台病毒是一种属于副粘病毒科呼吸道病毒属的病毒,Hemagglutinating Virus of Japan(HVJ)。正式名称为小鼠副流感1型病毒,是一种感染小鼠和大鼠并引起肺炎的RNA病毒。在癌症治疗中的开发,始于大阪大学的生物研究,主要由企业ジェノミディア开发的生物制剂HVJ-E最接近实际应用的基因治疗模型。这是一种以仙台病毒为骨骼的非病毒制剂基因治疗模型,曾进行过医师主导的前列腺癌治疗。但是参与开发的相关企业公布很难生产稳定的制剂。BioKnife® 是一种在保留仙台病毒骨架的同时开发的限制增殖的新制剂,由原ディナベック公司和九州大学联合开发。肿瘤特异性浸润性SeV载体删除了SeV载体中参与病毒颗粒形成的M基因,使感染该病毒的细胞内不形成病毒颗粒,生物刀的包膜蛋白在肿瘤细胞膜上积蓄,这种包膜蛋白预先设计为被肿瘤特异性蛋白酶激活,并通过肿瘤特异性蛋白酶发挥膜融合活性。这种膜融合活性诱导肿瘤细胞与相邻细胞之间的细胞融合,从而通过肿瘤细胞死亡的机制发挥抗肿瘤活性。这种包膜蛋白的存在可以重新激活肿瘤特异性蛋白酶,发挥膜融合作用。被激活的膜融合诱导癌细胞与周围细胞融合来发挥杀灭癌细胞的作用。现在,该制剂由ID制药主导开发,在动物实验中证实其有延长胸部恶性间皮瘤、脑肿瘤大鼠生存期的效果,也证实了其可以抑制肿瘤特异蛋白酶高表达的肺癌、胰腺癌、肾癌的动物模型肿瘤增殖。将仙台病毒作为生物刀可能对多种恶性肿瘤有效,可期待其能改善标准治疗失败或复发患者的生存。
4.痘苗病毒
アステラス制药与鸟取大学共同开发的痘苗病毒ASP9801正在美国进行Ⅰ期临床试验。众所周知,牛痘疫苗具有很高的安全性。本制剂在牛痘疫苗的基础上搭载了IL-7和IL-12,激发非特意性肿瘤免疫反应。病毒特意性地于癌细胞增殖,诱导癌细胞融合、溃破。アステラス制药计划在美国、日本、中国启动该病毒制剂的临床试验。


