胰腺癌药物治疗的进展
随着世界人口老龄化日益严重,胰腺癌患者的数量不断增加,目前已经超过肝癌,成为死亡人数排名第四的癌种。日本国立癌症中心医院肝胆胰内科主任奥坂拓志和日本杏林大学肿瘤学教授古瀬純司对世界各国胰腺癌药物治疗的临床数据进行了回顾性研究,并将研究结果发表在《美国胃肠病学》杂志上 (2020; 55: 369-382)。
●术前辅助化疗:确立标准治疗方案仍需证据
奥坂拓志团队改善胰腺癌预后的研究如下:
(1)确立可切除胰腺癌的早期诊断方法
(2)确立复发/不可切除的晚期胰腺癌的非手术治疗方法。并在近年来的临床研究中表现出喜人的结果,新的标准治疗方法也在不断开发中。
胰腺癌根治性切除术后复发率高,预后极差。现阶段很多临床试验正在探索切除前后实施化疗和放化疗的治疗效果。这些实验结果表明,术后辅助化疗已被认定为标准治疗,但术前辅助化疗还是缺乏大规模随机对照试验(RCT)研究作为Ⅰ类证据支持。
在来自2019年度美国临床肿瘤学会胃肠道癌研讨会(ASCO-GI 2019)上的报告称,在日本,吉西他滨联合S-1的术前辅助化疗显著延长了可切除胰腺癌患者的总生存期(OS)。该结果来自Prep-02 / JSAP-05的II / III期随机试验(Jpn J Clin Oncol 2019; 49: 190-194)。同时发现,交界可切除胰腺癌病例也出现了总生存期延长的迹象。
此外, 2018年度美国临床肿瘤学会(ASCO 2018)报道,在荷兰进行的PREOPANC-1 / III期临床试验的结果表明,术前辅助化疗有助于延长胰腺癌患者的总生存期(OS)(J Clin Oncol 2020年2月27日线上版)。
对于交界可切除胰腺癌,包括《2019年胰腺癌治疗指南》的各国指南均建议术前辅助化疗,但尚无既定方案。正在进行的一些随机对照试验(RCT)中,日本的GABARNANCE II / III期试验正在比较吉西他滨联合nab-紫杉醇与S-1放化疗。有望成为标准疗法的新证据。
●术后辅助化疗:日本较常用S-1方案
上世纪90年代以来,有3项随机对照试验研究了仅手术切除和手术切除+术后辅助化疗的治疗效果。
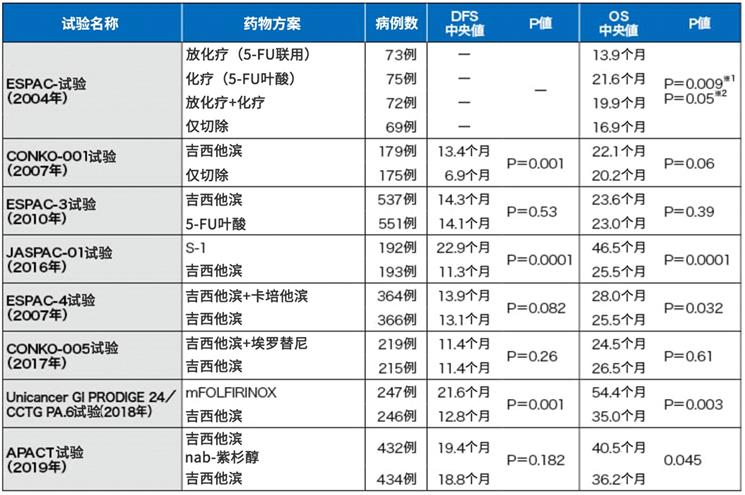
在德国和奥地利进行的III期CONKO-001试验的研究结果显示,术后吉西他滨辅助化疗显著延长了患者的无病生存期(DFS)(JAMA 2007; 297: 267-277))。长期随访后发现患者的总生存期(OS)也得到了显著改善(JAMA 2013; 310: 1473-1481)。
在日本进行的JSAP-02 / III期试验显示了同样的研究结果(Br J Cancer 2009; 101: 908-915)。
在日本和欧洲等国实施的ESPAC-3 / III期试验对比了仅手术切除,术后氟尿嘧啶+叶酸辅助化疗,以及术后单用吉西他滨化疗三个组群。结果显示,术后辅助化疗可延长患者总生存期(OS),而且,术后单用吉西他滨化疗组的严重不良事件发生率也得到了显著降低(JAMA 2012; 308: 147-156)。
鉴于以上这些试验结果,吉西他滨被认为是术后辅助化疗的国际标准。
但是在日本的JASPAC 01 / III期试验结果显示,对比单用吉西他滨,单用S-1更加能显著延长总生存期(OS)(Lancet 2016; 388: 248-257)。而S-1尚未被欧美人群认可。
在欧美国家进行的ESPAC-4 / III期试验(Lancet 2017; 389: 1011-1024)结果显示,吉西他滨联用卡培他滨的组合,比单用吉西他滨更能有效延长总生存期(OS)。
在PRODIGE 24-ACCORD 24/CCTG PA 6 / III期试验(N Engl J Med 2018; 379: 2395-2406)中,结果显示mFOLFIRINOX(奥沙利铂、亚叶酸钙、伊立替康,5-FU)对比单用吉西他滨,无病生存期(DFS)和总生存期(OS)都得到了显著延长。但是,由于没有对比单用S-1、吉西他滨联用卡培他滨,以及mFOLFIRINOX的临床试验,因此尚不清楚哪个是术后辅助疗法的最佳方案。
综上所述,在欧美国家推荐使用吉西他滨联用卡培他滨方案,或mFOLFIRINOX方案。而日本则推荐S-1方案。
ASCO 2019发表的APACT / III期试验结果显示,nab-紫杉醇联用吉西他滨,对比单用吉西他滨,无病生存期(DFS)并未改善,但长期随访后的结果显示,该方案在改善总生存期(OS)上显示出了优越性。(J Clin Oncol 2019;37: abstract 4000)
图表1:胰腺癌术后辅助化疗的主要试验
●局部晚期胰腺癌:化疗和放化疗,哪个更有效?
包括日本在内的各国治疗指南中,针对局部晚期胰腺癌都推荐化疗或放化疗。但是哪个治疗效果最佳,尚未达到共识。
欧美国家推荐在放化疗前先诱导化疗(放疗前辅助使用化疗)。但是,研究诱导化疗是否有效的唯一随机对照试验JCOG1106/ II期试验的结果显示,S-1联用放化疗前追加诱导吉西他滨化疗与否,并没有显著的差别。但是总生存期(OS)有所缩短(Ann Oncol 2016; 27: abstract 621PD)。因此,日本的《胰腺癌治疗指南2019版》不推荐诱导化疗。
局部晚期胰腺癌与远处转移胰腺癌都是不可手术的胰腺癌。但是目前尚未建立针对局部晚期胰腺癌的治疗标准。因此默认远处转移胰腺癌的治疗标准也适用于局部晚期胰腺癌。
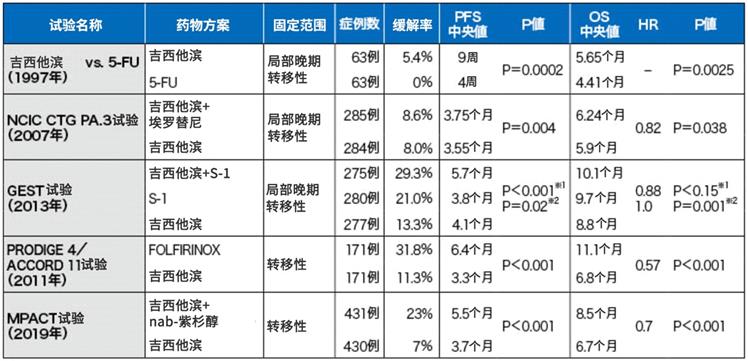
针对远处转移胰腺癌,FOLFIRINOX,吉西他滨联用nab-紫杉醇,都比单用吉西他滨更能有效改善预后。除英国外的各国治疗指南都推荐这两个方案。
在日本进行的JCOG1407/ II期试验是世界首个对比mFOLFIRINOX,吉西他滨联用nab-紫杉醇方案的随机对照试验(Pancreatology 2018; 18: 841-845)。计划在该研究的III期试验中还会对上述最佳方案和放化疗进行对比,以此制定标准治疗方法。
图表2:晚期胰腺癌一线治疗的关键试验
●转移性胰腺癌:推荐派姆单抗作为二线治疗药物用于微卫星高度不稳定的患者
针对远处转移胰腺癌的一线治疗,《2019年胰腺癌治疗指南》推荐了FOLFIRINOX方案和吉西他滨联用nab-紫杉醇方案。由于患者的身体状态或年龄等原因不适用时,推荐单用吉西他滨,或者单用S-1,或者吉西他滨联用埃罗替尼。海外III期试验证实了这些方案的有效性。之后日本也相继证实了各方案的有效性和安全性。
・FOLFIRINOX(N Engl J Med 2011; 364: 1817-1825)
・吉西他滨+nab-紫杉醇联用(N Engl J Med 2013; 369: 1691-1703)
・单用吉西他滨(J Clin Oncol 1997; 15: 2403-2413)
・吉西他滨+埃罗替尼联用(J Clin Oncol 2007; 25: 1960-1966)
另外,在日本和台湾进行的GEST/ III期试验的研究结果表明,S-1不逊于吉西他滨单药治疗(J Cancer Res Clin Oncol 2017; 143: 1053-1059)。在亚洲国家中,S-1单药治疗被作为标准治疗之一。
针对远处转移胰腺癌的二线治疗,《2019年胰腺癌治疗指南》推荐使用派姆单抗用于以下情况。
①先采用吉西他滨为基础的方案后,再采用氟尿嘧啶为基础的方案
②先采用氟尿嘧啶为基础的方案后,再采用吉西他滨为基础的方案
③微卫星高度不稳定(MSI-H)
在以NTRK融合基因阳性为研究对象的3项试验(STARTRK-2、STARTRK-1、ALKA-372-001)的综合分析中,欧州临床肿瘤学会(ESMO 2019)发表,ROS1/TRK抑制剂恩曲替尼有效(Ann Oncol 2018; 29: abstract LBA4)。该药物于2019年6月在日本被批准。但是NTRK阳性胰腺癌非常罕见,不足胰腺癌患者的1%。
●免疫疗法:通过改善肿瘤微环境来改善治疗效果
PD-1/PD-L1/CTLA-4都在激活T细胞,从而抑制肿瘤细胞中担当着重要角色。尤其是在恶性黑色素瘤等高免疫原性的肿瘤中,免疫检查点抑制剂(ICI)具有很好的效果。
针对胰腺癌的治疗,对比ICI单用和ICI联用的几个临床试验正在进行。但是治疗成绩并不理想。因此,胰腺癌的免疫治疗只能作为联合标准化疗使用的辅助治疗。然而,在一项针对微卫星高度不稳定(MSI-H)的研究中,派姆单抗已经取得了令人鼓舞的结果,并且有望在胰腺癌治疗中使用。
肿瘤浸润淋巴细胞(TIL)缺乏是ICI对胰腺癌无效的原因之一。因此,靶向TIL增殖或靶向肿瘤微环境的药物与ICI组合的治疗方法正在研发中。
抑制抗肿瘤免疫力的肿瘤浸润调节性T细胞(Treg)高度表达趋化因子受体CCR4,在实体瘤患者的纳武单抗和CCR4抗体 Mogamulizumab的I期试验中,已显示出了抗肿瘤活性和安全性(Clin Cancer Res 2019; 25: 6614-6622)。
在胰腺癌中,抑制T细胞抗肿瘤活性的肿瘤相关巨噬细胞(TAM)高度浸润,而集落刺激因子1受体(CSF-1R)参与TAM的维持与分化。因此抑制CSF-1R可导致ICI效应增强。对比胰腺癌治疗的纳武单抗和CSF-1R抗体cabiralizumab的I期试验结果显示,CSF-1R抗体cabiralizumab实现了部分缓解(PR)(J Clin Oncol 2018; 36: abstract 3020、J Immunother Cancer 2017; 5: abstract O42)。是否联合化疗的II期试验正在进行,以检验两种药物分别在有或没有化疗的情况下的疗效。(J Clin Oncol 2019; 37: abstract TPS465)。
TGFβ是一种抑制抗肿瘤免疫的细胞因子。在对比PD-L1抗体和TGFβ抑制剂的M7824/I期试验中,TGFβ抑制剂在胰腺癌治疗中,实现了部分缓解(PR)和疾病稳定(SD)。(Clin Cancer Res 2018; 24: 1287-1295)。
尽管在日本已经积极开展了使用肽疫苗进行免疫疗法的临床研究,但是对比单用吉西他滨,吉西他滨联用WT1多肽疫苗更加能够显著改善无进展生存期(PFS),这点在II期试验中已经得到了验证(Cancer Immunol Res 2018; 6: 320-331)。针对化疗不敏感的胰腺癌,S-1联用WT1的III期试验正在进行(Trials 2019; 20: 242)。在海外,免疫组合疗法(CRS-207 + GVAX Pancreas) 的效果已经获得了喜人结果(J Clin Oncol 2015; 33: 1325-1333)。
此外,针对胰腺癌的嵌合抗原受体T细胞CAR-T的免疫疗法的临床试验也在进行,结果值得期待。(Gastroenterology 2018; 155: 29-32)。
●靶向治疗:PARP抑制剂对BRCA1/BRCA2突变有效
胰腺癌的驱动基因包括KRAS,CDKN2A,TP53,SMAD4等,但目前的治疗靶点仅限于KRAS G12C和CDKN2A,基于基因突变的治疗方案尚未成为标准治疗。
参与DNA修复的基因突变(例如BRCA1 / 2,PALB2,ATM,ATR和ATRX)是最常见的突变,并且有相应的治疗药物。Ⅲ期POLO研究中,对于铂类为基础化疗无进展的BCRA1/2胚系突变转移性胰腺癌患者,PARP抑制剂奥拉帕尼的维持治疗可以显著延长无进展生存期(PFS)。(N Engl J Med 2019; 381: 317-327、「胰腺癌进入靶向治疗新时代」)
基于该试验结果,美国国立综合癌症网络NCCN的胰腺癌治疗指南中,将奥拉帕尼作为铂类为基础化疗无进展的BCRA1/2胚系突变转移性胰腺癌患者的维持治疗。另外,维利帕尼 ,瑞卡帕布等PARP抑制剂尚在临床试验中。
另外有报导称,在胰腺癌中,除了BRAF或EGFR突变,也会发现一些融合基因(FGFR、ALK、NTRK、NRG1等)的突变(Clin Cancer Res 2018; 24: 1344-1354)。在最新的NCCN胰腺癌指南中,“推荐使用全面的基因检测来进行胚系突变检测,以识别遗传性癌症综合征。”,“局部晚期或转移性胰腺癌,推荐行肿瘤/体细胞基因分析。”
●其他:液体活检对检测微小残留病变非常重要。
奥坂团队最后还提到了应用液体活检的可能性。液体活检对血液中的循环肿瘤细胞(CTC)和循环肿瘤DNA (ctDNA),以及外泌体进行监测。液体活检是微创检测,而且还具有以下优势。
1、可以预测预后
2、可以及时监测治疗反应和复发
3、寻找治疗靶点
4、研究转移癌的生物学特性和耐药机制,有助于新药开发。
液体活检有望作为一种生物标记物检测手段,应用于胰腺癌早期筛查和靶向治疗。
奥坂还指出,对切除后微小残留病变的检测和诊断是今后研究的另外一个重要课题。


